Método Kjeldahl
[4]Es el método oficial, descrito en múltiples normativas: AOAC, USEPA, ISO, DIN, Farmacopeas y distintas Directivas Comunitarias.
En una primera etapa, la muestra es descompuesta en ácido sulfúrico caliente y concentrado para mineralizar la materia orgánica y convertir el nitrógeno que forma parte de proteínas o ácidos nucleicos, en ion amonio.
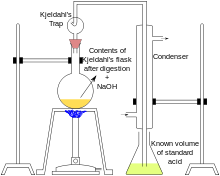
En la segunda etapa, cuando toda la materia orgánica ha sido descompuesta, la disolución resultante es enfriada, diluida y se hace básica, un proceso que convierte los iones amonio en amoniaco que debe ser destilado evitando cualquier perdida de esta sustancia volátil, por lo que se recoge en una disolución ácida.
Para esta digestión en el laboratorio se utiliza ácido sulfúrico concentrado que es necesario elevar a altas temperaturas, por lo que, generalmente, se añade sulfato de potasio.
Además, se añaden catalizadores que facilitan el proceso de digestión.
Como catalizadores se utilizan compuestos de mercurio, cobre o selenio.
En este proceso la materia orgánica se carboniza dando lugar a la formación de una espuma negra.
[7] Las proteínas se hidrolizan convirtiéndose en aminoácidos o en aminas, las cuales terminan como derivados del amonio.
En cambio, los compuestos con grupos nitro, azo y azoxi son propensos a pasar al estado elemental o a sus diversos óxidos, sin convertirse en ion amonio, lo que implica que este nitrógeno no es contabilizado en la etapa de valoración.
Algunas muestras pueden requerir periodos de calentamiento superiores a una o dos horas.
Dada la volatilidad del amoniaco (es un gas), para evitar pérdidas, la salida del condensador se sumerge en el matraz receptor del destilado, que contiene una disolución ácida, con la que reacciona inmediatamente, formando nuevamente ion amonio (NH4+) , no volátil, con lo que queda absorbido en la disolución ácida.
También se utiliza el método Kjeldahl para la determinación de nitrógeno en aguas residuales, suelos, fertilizantes y otros materiales.